.
Egzamin maturalny z chemii na poziomie podstawowym rozpocznie się we wtorek o godz. 9. Uczniowie będą mieli 120 minut na rozwiązanie testu. Stawką jest 50 punktów do zdobycia.
We wtorek maturzyści stają również:
Chemia - rozszerzony [ARKUSZ, ODPOWIEDZI]
Równocześnie o tej samej godzinie startuje egzamin z chemii na poziomie rozszerzonym. Tutaj maturzyści mają pół godziny więcej na rozwiązanie, a maksymalna liczba punktów to 60. Arkusze i odpowiedzi będą dostępne na naszych stronach około godz. 14.
Drugi tydzień matur będzie upływał pod znakiem przedmiotów dodatkowych. Punkty za te przedmioty są ważne w kontekście rekrutacji na studia. Uczniowie mogą wybrać pomiędzy biologią, geografią, historią, wiedzą o społeczeństwie, filozofią, chemią czy fizyką z astronomią.
Matura 2013: Chemia - poziom podstawowy
ODPOWIEDZI
PRZYKŁADOWE ODPOWIEDZI - CHEMIA - POZIOM PODSTAWOWY
ZADANIE 1
1. Atom bromu ma 7 elektronów walencyjnych, które w stanie podstawowym znajdują się w czwartej powłoce. PRAWDA
2. Najwyższy stopień utlenienia, jaki przyjmuje brom w związkach chemicznych, wynosi VII. PRAWDA
3. Brom jest niemetalem aktywniejszym od chloru. FAŁSZ
ZADANIE 2
Liczba masowa
izotopu I - 40u
izotopu II - 45u
ZADANIE 3
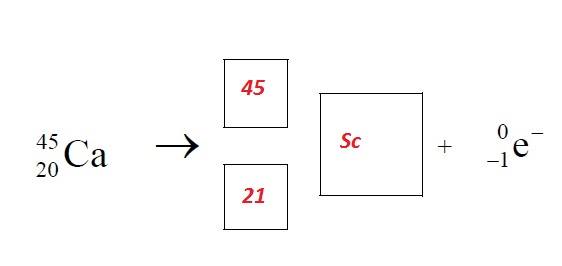
ZADANIE 4
ZADANIE 5
zestaw C
ZADANIE 6
ZADANIE 7
ZADANIE 8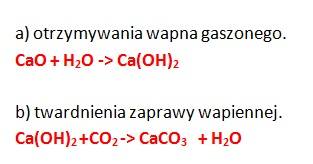
ZADANIE 9
Reakcja otrzymywania wapna gaszonego jest przemianą egzotermiczną, co oznacza, że podczas tej przemiany energia w postaci ciepła jest wydzielana.
ZADANIE 10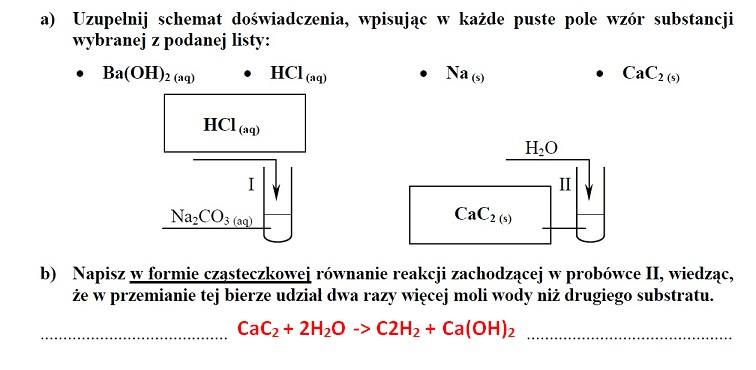
ZADANIE 11
Barwa wskaźnika: malinowa
Odczyn powstałego roztworu: zasadowy
ZADANIE 12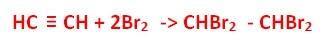
ZADANIE 13
ODPOWIEDŹ: Procentowa zawartość cynku w tombaku wynosi 80,4 %.
ZADANIE 14
1. Po dodaniu 90 gramów glukozy do 100 gramów wody o temperaturze 18°C i ogrzaniu całości do temperatury 25°C otrzymano roztwór nienasycony.
2. Stężenie procentowe (w procentach masowych) nasyconego wodnego roztworu glukozy jest równe 47,6% w temperaturze około 20°C.
ZADANIE 15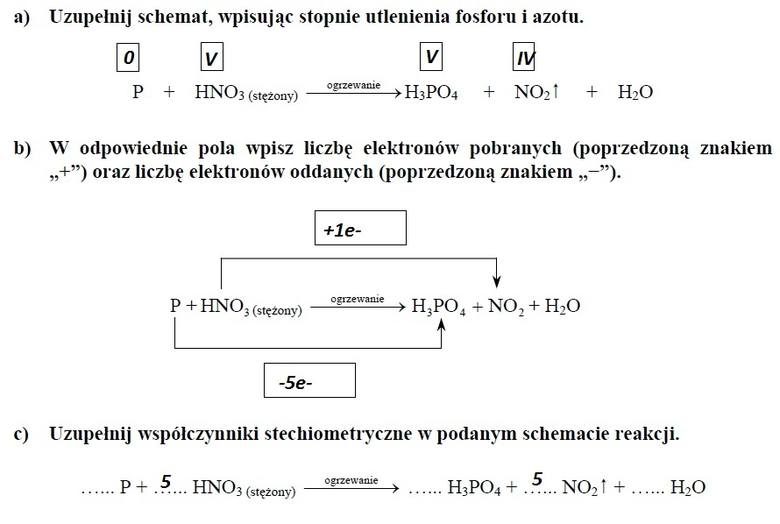
ZADANIE 16
1. W opisanej przemianie fosfor jest reduktorem, a kwas azotowy utleniaczem. PRAWDA
2. W opisanej przemianie stopień utlenienia fosforu obniża się. FAŁSZ
3. W opisanej przemianie fosfor ulega procesowi utleniania, oddając elektrony. PRAWDA
ZADANIE 17
Probówka I: bezbarwny
Probówka II: czerwony
ZADANIE 18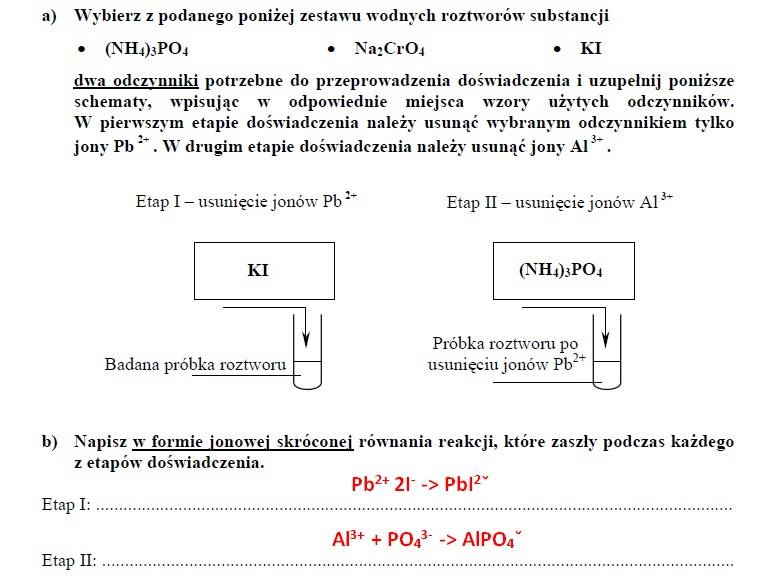
ZADANIE 19
2,2-dimetylopropan
ZADANIE 20
Związek oznaczony numerem I
B. tworzy dwie monochloropochodne.
ZADANIE 21
3,3 - dimetylobut - 1-en
ZADANIE 22
1. Homologami są związki oznaczone numerami III i V.
2. Izomerami są związki oznaczone numerami II i VI.
3. Butan powstaje w wyniku reakcji uwodornienia związku oznaczonego numerem III.
4. Utlenienie butan-2-olu prowadzi do otrzymania związku oznaczonego numerem VI.
5. Powstanie ceglastej substancji stałej można zaobserwować po ogrzaniu mieszaniny wodorotlenku miedzi(II) ze związkiem oznaczonym numerem II.
ZADANIE 23
Związek A należy do szeregu homologicznego alkiny
Związek B należy do szeregu homologicznego alkany
ZADANIE 24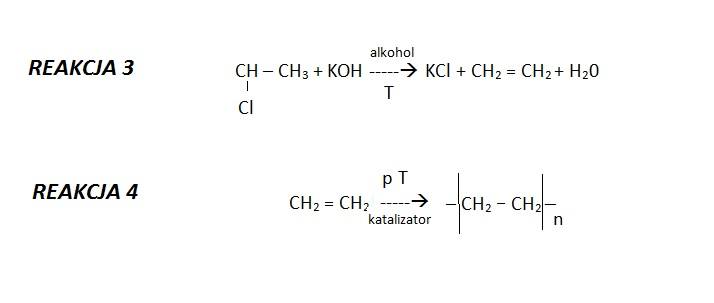
ZADANIE 25
Polietylen jest niereaktywnym związkiem organicznym używanym do produkcji artykułów codziennego użytku. Jest tworzywem palnym, które charakteryzuje się podatnością na barwienie i formowanie.
ZADANIE 26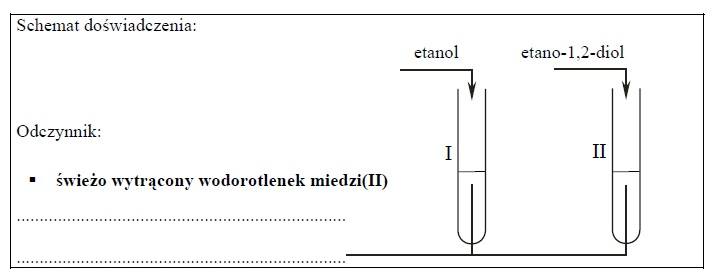
Probówka I: brak objawów reakcji
Probówka II: pojawia się szafirowe zabarwienie. Powstaje barwny roztwór
ZADANIE 27
ZADANIE 28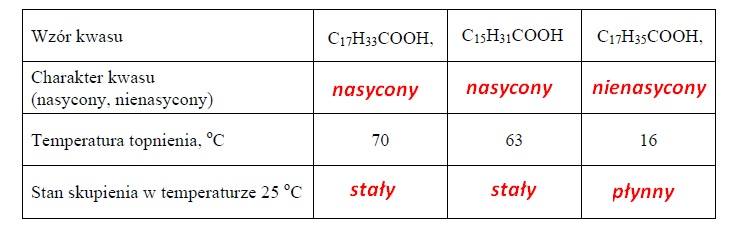
ZADANIE 29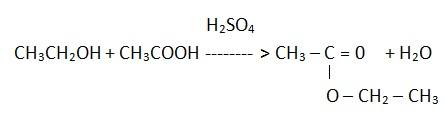
a) Ustal liczbę atomów węgla w cząsteczce opisanego estru.
4
ZADANIE 30
1. Związek X to substancja organiczna, która powstaje w wyniku reakcji nitrowania benzenu. PRAWDA
2. Związek organiczny otrzymany w wyniku redukcji związku X to amina aromatyczna o wzorze sumarycznym C6H7N. PRAWDA
3. Związek organiczny otrzymany w wyniku redukcji związku X nie reaguje z kwasem solnym, co potwierdza jego kwasowy charakter. FAŁSZ
ZADANIE 31
W celu przygotowania 0,5 dm3 wodnego roztworu glukozy o stężeniu 0,25 mol·dm-3 należy odważyć 22,5g glukozy. Odważoną próbkę glukozy należy przenieść do kolby miarowej o pojemności 500cm3 i dodać niewielką ilość wody w celu rozpuszczenia substancji. Następnie zawartość naczynia należy dopełnić 500cm3 do kreski znajdującej się na szyjce kolby miarowej.
Upalne dni bez stresu. Praktyczne sposoby na zdrowe lato
Dołącz do nas na Facebooku!
Publikujemy najciekawsze artykuły, wydarzenia i konkursy. Jesteśmy tam gdzie nasi czytelnicy!
Dołącz do nas na X!
Codziennie informujemy o ciekawostkach i aktualnych wydarzeniach.
Kontakt z redakcją
Byłeś świadkiem ważnego zdarzenia? Widziałeś coś interesującego? Zrobiłeś ciekawe zdjęcie lub wideo?









